Изохинолин
| Изохинолин | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование | бензо[c]пиридин |
| Хим. формула | C9H7N |
| Физические свойства | |
| Молярная масса | 129,16 г/моль |
| Термические свойства | |
| Т. плав. | 25,5 °C |
| Т. кип. | 243,25 °C |
| Тройная точка | K ( °C), Па |
| Кр. точка | K ( °C), Па |
| Химические свойства | |
| pKa | 5,40 |
| Классификация | |
| Рег. номер CAS | 119-65-3 |
| PubChem | 8405 |
| Рег. номер EINECS | 204-341-8 |
| SMILES | C1=CC=C2C=NC=CC2=C1 |
| InChI | 1S/C9H7N/c1-2-4-9-7-10-6-5-8(9)3-1/h1-7H AWJUIBRHMBBTKR-UHFFFAOYSA-N |
| ChEBI | 16092 и 43484 |
| ChemSpider | 8098 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Изохинолин — гетероциклическое органическое соединение состава C9H7N.
Содержание
1 Свойства
2 Получение
3 Применение
4 Литература
Свойства |
Бесцветные кристаллы со слабым запахом миндаля;Тпл=24,5 °C, Ткип=243 °C. Изохинолин плохо растворим в холодной воде, в органических растворителях — хорошо. Он содержится в небольшом количестве в каменноугольном дёгте, откуда его выделяют вместе с хинолином. Изохинолин — более сильное основание, чем хинолин.
При протонировании изохинолин образует соли изохинолиния; с алкил-, ацил-, арилгалогенидами и диметилсульфатом образует четвертичные соли.
При гидрировании над платиной превращается в 1,2,3,4-тетрагидроизохинолин; при полном гидрировании — в цис-декагидроизохинолин.
Окисление смесью озона и кислорода приводит к пиридин-3,4-дикарбоновой кислоте (цинхомероновая кислота), окисление пероксокислотами ведёт к изохинолин-N-оксиду.
Реакции электрофильного замещения происходят в положении 5. Бромирование легче протекает в присутствии AlCl3, нитрование идёт при действии серной и азотной кислот. Сульфирование при действии 40%-ного олеума при температуре 180оС приводит обычно к изохинолин-8-сульфокислоте. Сульфирование 60%-ной серной кислотой при 300оС ведёт к смеси изохинолин-5- и изохинолин-8-сульфокислот.
При высокой температуре изохинолин вступает в реакции бромирования по радикальному механизму с образованием 1-бромизохинолина.
Нуклеофильное замещение протекает как правило в положение 1. С гидроксидом калия при 200оС изохинолин образует 1-гидроксиизохинолин, с амидом натрия — 1-аминоизохинолин.
Получение |
Важнейший метод получения изохинолина и его производных — циклодегидратация β-фенилэтиламидов кислот C6H5CH2CH2NHCOR (реакция Бишлера — Напиральского) с последующим дегидрированием образующихся 3,4-дигидроизохинолинов.
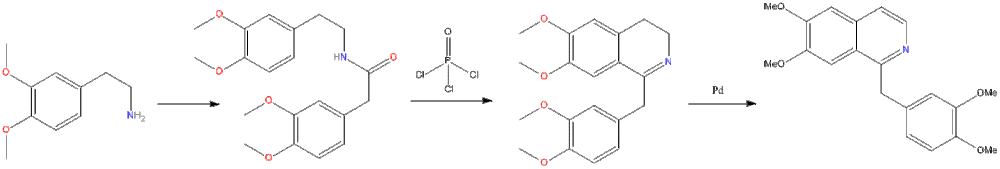
Другие методы синтеза изохинолина и его производных: метод Померанца — Фрича (конденсация ацетофенона с а-аминоацетацеталем); метод Пикте — Шпенглера.
Применение |
Изохинолин служит исходным продуктом при синтезе сенсибилизирующих красителей (например, изохинолинового красного и лекарственных средств.
Изохинолиновое ядро входит в структуру ряда важных алкалоидов (папаверина, морфина, кодеина, курарина и др.).
Литература |
- Даффа реакция — Меди// Химическая энциклопедия в 5 томах. — М.: Большая Российская Энциклопедия, 1990. — Т. 2. — 671 с.