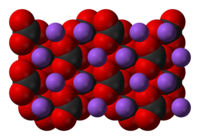
Карбонат натрия
| Карбонат натрия | |
|---|---|
  | |
 | |
| Общие | |
| Систематическое наименование | Карбонат натрия |
| Традиционные названия | кальцинированная сода, углекислый натрий |
| Хим. формула | Na2CO3 |
| Физические свойства | |
| Молярная масса | 105,99 г/моль |
| Плотность | 2,53 г/см³ |
| Термические свойства | |
| Т. плав. | 852 °C |
| Т. кип. | 1600 °C |
| Химические свойства | |
| pKa | 10,33 |
Растворимость в воде при 20 °C | 21,8 г/100 мл |
| Классификация | |
| Рег. номер CAS | 497-19-8 |
| PubChem | 10340 |
| Рег. номер EINECS | 207-838-8 |
| SMILES | C(=O)([O-])[O-].[Na+].[Na+] |
| InChI | 1S/CH2O3.2Na/c2-1(3)4;;/h(H2,2,3,4);;/q;2*+1/p-2 CDBYLPFSWZWCQE-UHFFFAOYSA-L |
| Кодекс Алиментариус | E500(i) |
| RTECS | VZ4050000 |
| ChEBI | 29377 |
| ChemSpider | 9916 |
| Безопасность | |
| ЛД50 | 4 г/кг (крысы, орально) |
| Пиктограммы СГС |  |
| NFPA 704 |  0 1 0 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Карбона́т на́трия Na2CO3 (другие названия — кальцинированная сода) — химическое соединение, натриевая соль угольной кислоты.
Содержание
1 Тривиальные названия
2 Оксиды и гидроксиды
3 Нахождение в природе
4 Получение
4.1 Способ Леблана
4.2 Промышленный аммиачный способ (способ Сольве)
4.3 Способ Хоу
4.3.1 Сравнение способов
5 Свойства
6 Безопасность
7 Применение
8 Примечания
9 Литература
Тривиальные названия |
Сода — общее название технических натриевых солей угольной кислоты.
- Na2CO3 (карбонат натрия) — кальцинированная сода, бельевая сода
- Na2CO3·10H2O (декагидрат карбоната натрия, содержит 62,5 % кристаллизационной воды) — стиральная сода; иногда выпускается в виде Na2CO3·H2O или Na2CO3·7H2O
- NaHCO3 (гидрокарбонат натрия) — пищевая сода, натрий двууглекислый (устар.), бикарбонат натрия
«Сода» в европейских языках происходит, вероятно, от арабского "suwwad" - общего названия различных видов солянок, растений, из золы которых её добывали в средние века; существуют и другие версии [1]. Кальцинированная сода (карбонат натрия) называется так потому, что для получения её из бикарбоната последний "кальцинируют" (лат. calcinatio, от calx, по сходству с процессом обжига извести), то есть прокаливают.
Оксиды и гидроксиды |
| Вид | Для Na | Для С |
|---|---|---|
| Гидроксид | NaOH | H2CO3 |
| Оксид | Na2O | CO2 |
Нахождение в природе |
В природе сода встречается в золе некоторых морских водорослей, а также в виде минералов:
нахколит NaHCO3
трона Na2CO3·NaHCO3·2H2O
натрит (сода) Na2CO3·10H2O
термонатрит Na2CO3·Н2O.
Современные содовые озёра известны в Забайкалье и в Западной Сибири; большой известностью пользуется озеро Натрон в Танзании и озеро Сирлс в Калифорнии[2]. Трона, имеющая промышленное значение, открыта в 1938 в составе эоценовой толщи Грин-Ривер (Вайоминг, США). Вместе с троной в этой осадочной толще обнаружено много ранее считавшихся редкими минералов, в том числе давсонит, который рассматривается как сырьё для получения соды и глинозёма. В США природная сода удовлетворяет более 40 % потребности страны в этом полезном ископаемом.
Получение |
До начала XIX века карбонат натрия получали преимущественно из золы некоторых морских водорослей, прибрежных и солончаковых растений путём перекристаллизации относительно малорастворимого NaHCO3 из щёлока.
Способ Леблана |
В 1791 году французский химик Никола Леблан получил патент на «Способ превращения глауберовой соли в соду». По этому способу при температуре около 1000 °C запекается смесь сульфата натрия («глауберовой соли»), мела или известняка (карбоната кальция) и древесного угля. Уголь восстанавливает сульфат натрия до сульфида:
- Na2SO4+2C→Na2S+2CO2{displaystyle {mathsf {Na_{2}SO_{4}+2Crightarrow Na_{2}S+2CO_{2}}}}
- Na2SO4+2C→Na2S+2CO2{displaystyle {mathsf {Na_{2}SO_{4}+2Crightarrow Na_{2}S+2CO_{2}}}}
Сульфид натрия реагирует с карбонатом кальция:
- Na2S+CaCO3→Na2CO3+CaS{displaystyle {mathsf {Na_{2}S+CaCO_{3}rightarrow Na_{2}CO_{3}+CaS}}}
- Na2S+CaCO3→Na2CO3+CaS{displaystyle {mathsf {Na_{2}S+CaCO_{3}rightarrow Na_{2}CO_{3}+CaS}}}
Полученный расплав обрабатывают водой, при этом карбонат натрия переходит в раствор, сульфид кальция отфильтровывают, затем раствор карбоната натрия упаривают. Сырую соду очищают перекристаллизацией. Процесс Леблана даёт соду в виде кристаллогидрата (см. выше), поэтому полученную соду обезвоживают кальцинированием.
Сульфат натрия получали обработкой каменной соли (хлорида натрия) серной кислотой:
- 2NaCl+H2SO4→Na2SO4+2HCl{displaystyle {mathsf {2NaCl+H_{2}SO_{4}rightarrow Na_{2}SO_{4}+2HCl}}}
- 2NaCl+H2SO4→Na2SO4+2HCl{displaystyle {mathsf {2NaCl+H_{2}SO_{4}rightarrow Na_{2}SO_{4}+2HCl}}}
Выделявшийся в ходе реакции хлороводород улавливали водой с получением соляной кислоты.
Первый содовый завод такого типа в России был основан промышленником М. Прангом и появился в Барнауле в 1864 году.
После появления более экономичного (не остаётся в больших количествах побочный сульфид кальция) и технологичного способа Сольве, заводы, работающие по способу Леблана, стали закрываться. К 1900 году 90 % предприятий производили соду по методу Сольве, а последние фабрики, работающие по методу Леблана, закрылись в начале 1920-х.
Промышленный аммиачный способ (способ Сольве) |

Карбонат натрия
В 1861 году бельгийский инженер-химик Эрнест Сольве запатентовал метод производства соды, который используется и по сей день.
В насыщенный раствор хлорида натрия пропускают эквимолярные количества газообразных аммиака и диоксида углерода, то есть как бы вводят гидрокарбонат аммония NH4HCO3:
- NH3+CO2+H2O+NaCl→NaHCO3+NH4Cl{displaystyle {mathsf {NH_{3}+CO_{2}+H_{2}O+NaClrightarrow NaHCO_{3}+NH_{4}Cl}}}
- NH3+CO2+H2O+NaCl→NaHCO3+NH4Cl{displaystyle {mathsf {NH_{3}+CO_{2}+H_{2}O+NaClrightarrow NaHCO_{3}+NH_{4}Cl}}}
Выпавший остаток малорастворимого (9,6 г на 100 г воды при 20 °C) гидрокарбоната натрия отфильтровывают и кальцинируют (обезвоживают) нагреванием до 140—160 °C, при этом он переходит в карбонат натрия:
- 2NaHCO3→otNa2CO3+H2O+CO2↑{displaystyle {mathsf {2NaHCO_{3}{xrightarrow[{}]{^{o}t}}Na_{2}CO_{3}+H_{2}O+CO_{2}uparrow }}}
- 2NaHCO3→otNa2CO3+H2O+CO2↑{displaystyle {mathsf {2NaHCO_{3}{xrightarrow[{}]{^{o}t}}Na_{2}CO_{3}+H_{2}O+CO_{2}uparrow }}}
Образовавшийся CO2 возвращают в производственный цикл. Хлорид аммония NH4Cl обрабатывают гидроксидом кальция Ca(OH)2:
- 2NH4Cl+Ca(OH)2→CaCl2+2NH3+2H2O{displaystyle {mathsf {2NH_{4}Cl+Ca(OH)_{2}rightarrow CaCl_{2}+2NH_{3}+2H_{2}O}}}
- 2NH4Cl+Ca(OH)2→CaCl2+2NH3+2H2O{displaystyle {mathsf {2NH_{4}Cl+Ca(OH)_{2}rightarrow CaCl_{2}+2NH_{3}+2H_{2}O}}}
Полученный NH3 также возвращают в производственный цикл.
Таким образом, единственным отходом производства является хлорид кальция.
Первый содовый завод такого типа в мире был открыт в 1863 в Бельгии; первый завод такого типа в России был основан в районе уральского города Березники фирмой «Любимов, Сольве и Ко» в 1883 году. Его производительность составляла 20 тысяч тонн соды в год. В 2010 году ФАС России отказала фирме Solvay в покупке этого завода, разрешив покупку группе Башкирская химия (ей также принадлежит завод Сода).[источник не указан 2535 дней]
До сих пор этот способ остаётся основным способом получения соды во всех странах.
Способ Хоу |
Разработан китайским химиком Хоу (Hou Debang) в 1930-х годах. Отличается от процесса Сольве тем, что не использует гидроксид кальция.
По способу Хоу в раствор хлорида натрия при температуре 40 градусов подается диоксид углерода и аммиак. Менее растворимый гидрокарбонат натрия в ходе реакции выпадает в осадок (как и в методе Сольве). Затем раствор охлаждают до 10 градусов. При этом выпадает в осадок хлорид аммония, а раствор используют повторно для производства следующих порций соды.
Сравнение способов |
По методу Хоу в качестве побочного продукта образуется NH4Cl вместо CaCl2 по методу Сольве.
Способ Сольве был разработан до появления процесса Габера, в то время аммиак был в дефиците, поэтому регенерировать его из NH4Cl было необходимо. Метод Хоу появился позже, необходимость регенерации аммиака уже не стояла так остро, соответственно, аммиак можно было не извлекать, а использовать его как азотное удобрение в виде соединения NH4Cl.
Тем не менее NH4Cl содержит хлор, избыток которого вреден для многих растений, поэтому использование NH4Cl в качестве удобрения ограничено. В свою очередь рис хорошо переносит избыток хлора, и в Китае, где применяется NH4Cl для рисоводства, метод Хоу, дающий NH4Cl в качестве побочного продукта, более широко представлен по сравнению с другими регионами.
В настоящее время в ряде стран практически весь искусственно производящийся карбонат натрия вырабатывается по методу Сольве (включая метод Хоу как модификацию), а именно в Европе 94 % искусственно производимой соды, во всем мире — 84 % (2000 год)[3].
Свойства |
Кристаллогидраты карбоната натрия существуют в разных формах: бесцветный моноклинный Na2CO3·10H2O, при 32,017 °C переходит в бесцветный ромбический Na2CO3·7H2O, последний при нагревании до 35,27 °C бесцветный переходит в ромбический Na2CO3·H2O. В интервале 100-120 °C моногидрат теряет воду. Плавится при 852 °C.
Безводный карбонат натрия представляет собой бесцветный порошок.
| Параметр | Безводный карбонат натрия | Декагидрат Na2CO3·10H2O |
|---|---|---|
| Молекулярная масса | 105,99 а. е. м. | 286,14 а. е. м. |
| Температура плавления | 852 °C (по другим источникам, 853 °C) | 32 °C |
| Растворимость | Не растворим в ацетоне, и сероуглероде, малорастворим в этаноле, хорошо растворим в глицерине и воде | |
| Плотность ρ | 2,53 г/см³ (при 20 °C) | 1,446 г/см³ (при 17 °C) |
Стандартная энтальпия образования ΔH | −1131 кДж/моль (т) (при 297 К) | −4083,5 кДж/моль ((т) (при 297 К) |
Стандартная энергия Гиббса образования G | −1047,5 кДж/моль (т) (при 297 К) | −3242,3 кДж/моль ((т) (при 297 К) |
Стандартная энтропия образования S | 136,4 Дж/моль·K (т) (при 297 К) | |
| Стандартная мольная теплоёмкость Cp | 109,2 Дж/моль·K (жг) (при 297 К) |
Температура, °C | 0 | 10 | 20 | 25 | 30 | 40 | 50 | 60 | 80 | 100 | 120 | 140 |
Растворимость, г Na2CO3 на 100 г H2O | 7 | 12,2 | 21,8 | 29,4 | 39,7 | 48,8 | 47,3 | 46,4 | 45,1 | 44,7 | 42,7 | 39,3 |
В водном растворе карбонат натрия гидролизуется, что обеспечивает щелочную реакцию среды. Уравнение гидролиза (в ионной форме):
- CO32−+H2O⇄HCO3−+OH−{displaystyle {mathsf {CO_{3}^{2-}+H_{2}Orightleftarrows HCO_{3}^{-}+OH^{-}}}}
- CO32−+H2O⇄HCO3−+OH−{displaystyle {mathsf {CO_{3}^{2-}+H_{2}Orightleftarrows HCO_{3}^{-}+OH^{-}}}}
Первая константа диссоциации угольной кислоты равна 4,5⋅10−7. Все кислоты, более сильные, чем угольная, вытесняют её в реакции с карбонатом натрия. Так как угольная кислота крайне нестойкая, она тут же разлагается на воду и углекислый газ:
- Na2CO3+H2SO4→Na2SO4+H2O+CO2↑{displaystyle {mathsf {Na_{2}CO_{3}+H_{2}SO_{4}rightarrow Na_{2}SO_{4}+H_{2}O+CO_{2}uparrow }}}
- Na2CO3+H2SO4→Na2SO4+H2O+CO2↑{displaystyle {mathsf {Na_{2}CO_{3}+H_{2}SO_{4}rightarrow Na_{2}SO_{4}+H_{2}O+CO_{2}uparrow }}}
Безопасность |
Кальцинированная сода относится к веществам 3-го класса опасности. Аэрозоль кальцинированной соды при попадании на влажную кожу и слизистые оболочки глаз и носа может вызвать раздражение, а при длительном воздействии ее – дерматит. Предельно допустимая концентрация аэрозоли кальцинированной соды в воздухе производственных помещений - 2 мг/м3.
Применение |
.mw-parser-output .ts-Родственные_проекты{background:#f8f9fa;border:1px solid #a2a9b1;clear:right;float:right;font-size:90%;margin:0 0 1em 1em;padding:.5em .75em}.mw-parser-output .ts-Родственные_проекты th,.mw-parser-output .ts-Родственные_проекты td{padding:.25em 0;vertical-align:middle}.mw-parser-output .ts-Родственные_проекты td{padding-left:.5em}
Карбонат натрия на Викискладе |
Карбонат натрия используют в стекольном производстве; мыловарении и производстве стиральных и чистящих порошков; эмалей, для получения ультрамарина. Также он применяется для смягчения воды паровых котлов и вообще уменьшения жёсткости воды, для обезжиривания металлов и десульфатизации доменного чугуна. Карбонат натрия — исходный продукт для получения NaOH, Na2B4O7, Na2HPO4. Может использоваться в сигаретных фильтрах[4].
В пищевой промышленности карбонаты натрия зарегистрированы в качестве пищевой добавки E500, — регулятора кислотности, разрыхлителя, препятствующего комкованию и слёживанию. Карбонат натрия (кальцинированная сода, Na2CO3) имеет код 500i, гидрокарбонат натрия (пищевая сода, NaHCO3) — 500ii, их смесь — 500iii.
Одна из новейших технологий повышения нефтеотдачи пластов — АСП заводнение, в котором применяется сода в сочетании с ПАВ для снижения межфазного натяжения между водой и нефтью
Также используется для приготовления фотографических проявителей как ускоряющее средство[5].
Самостоятельно добавляется в моторное масло для предотвращения полимеризации. Концентрация 2 г на 1л масла.
Примечания |
↑ “Soda”: An etymological “headache”?
↑ https://books.google.ru/books?id=p4p0DQAAQBAJ&pg=PT5&lpg=PT5&dq=%D0%BE%D0%B7%D0%B5%D1%80%D0%BE+%D0%A1%D0%B8%D1%80%D0%BB%D1%81+%D0%B2+%D0%9A%D0%B0%D0%BB%D0%B8%D1%84%D0%BE%D1%80%D0%BD%D0%B8%D0%B8.&source=bl&ots=L9JFwBw9I9&sig=ACfU3U2QQGTyDReRRJ-TMQ-NJhbBAPIq-w&hl=ru&sa=X&ved=2ahUKEwj-oubK_5zgAhUKKywKHQzTC8oQ6AEwBXoECAMQAQ#v=onepage&q=%D0%BE%D0%B7%D0%B5%D1%80%D0%BE%20%D0%A1%D0%B8%D1%80%D0%BB%D1%81%20%D0%B2%20%D0%9A%D0%B0%D0%BB%D0%B8%D1%84%D0%BE%D1%80%D0%BD%D0%B8%D0%B8.&f=false
↑ WebCite query result
↑ Патент на изобретение
↑ Гурлев, 1988, с. 298.
Литература |
- Гурлев Д.С. Справочник по фотографии (обработка фотоматериалов). — К.: Тэхника, 1988.
- ГОСТ 5100-85 Сода кальцинированная техническая. Технические условия (с Изменением N 1)




![{displaystyle {mathsf {2NaHCO_{3}{xrightarrow[{}]{^{o}t}}Na_{2}CO_{3}+H_{2}O+CO_{2}uparrow }}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5908963ccad7f278ec1e97ff1fbc8ece58a9096d)


